CIRI ATOMKARBON
HIDROKARBON
Hidrokarbon adalah
sebuah senyawa yang terdiri dari unsur karbon (C) dan
unsur hidrogen (H). Seluruh hidrokarbon memiliki rantai karbon dan
atom-atom hidrogen yang berikatan dengan rantai tersebut. Istilah tersebut
digunakan juga sebagai pengertian dari hidrokarbon alifatik.
Sebagai contoh, metana (gas rawa) adalah
hidrokarbon dengan satu atom karbon dan empat atom hidrogen: CH4. Etana adalah
hidrokarbon (lebih terperinci, sebuah alkana) yang terdiri dari dua atom karbon
bersatu dengan sebuah ikatan tunggal, masing-masing mengikat tiga atom karbon:
C2H6. Propana memiliki tiga atom C (C3H8)
dan seterusnya (CnH2·n+2).
KEKHASAN ATOM KARBON
Banyaknya jenis dan jumlah senyawa karbon tidak
terlepas dari sifat khas atom karbon yang dapat membentuk senyawa dengan
berbagai unsur dan dengan struktur yang bervariasi. Beberapa sifat khas atom
karbon tersebut antara lain :
1.
Konfigurasi elektron atom karbon
Atom
karbon mempunyai nomor atom 6, dengan 4 elektron valensi. Keempat elektron
valensi tersebut dapat membentuk pasangan elektron bersama dengan atom lain
membentuk ikatan kovalen. Keempat elektron valensi ini dapat digambarkan
sebagai tangan ikatan.
2. Cara atom karbon berikatan
Atom
karbon dengan keempat tangan tersebut dapat membentuk rantai karbon dengan
berbagai bentuk dan kemungkinan. Setiap kemungkinan menghasilkan satu jenis
senyawa. Semakin banyak kemungkinan semakin banyak jenis senyawa yang bisa
dibentuk oleh atom karbon. Beberapa kemungkinan rantai karbon yang dibentuk
dapat dikelompokkan berdasarkan :
a. Jenis ikatan
· Ikatan tunggal, yaitu
ikatan antara atom-atom karbon dengan satu tangan ikatan (sepasang elektron
ikatan) Ikatan rangkap dua, yaitu ikatan antara atom-atom
karbon dengan dua tangan ikatan (dua pasang elektron ikatan)
· Ikatan rangkap dua,
yaitu ikatan antara atom-atom karbon dengan dua tangan ikatan (dua pasang
elektron ikatan)
· Ikatan rangkap tiga,
yaitu ikatan antara atom-atom karbon dengan tiga tangan ikatan (tiga pasang
elektron ikatan)
a. Bentuk rantai
· Rantai terbuka
(alifatis), yaitu rantai yang antara ujung-ujung atom karbonnya tidak saling
berikatan. Rantai jenis ini ada yang bercabang dan ada yang tidak bercabang.
·
Rantai tertutup
(siklis),
3.
Posisi atom karbon di dalam rantai karbon
Berdasarkan jumlah atom karbon
lain yang diikat terdapat empat posisi atom karbon yaitu :
a.
Atom karbon primer, yaitu atom karbon yang mengikat satu atom karbon
yang lainnya.
b.
Atom karbon sekunder, yaitu atom karbon yang mengikat dua atom karbon
lainnya.
c.
Atom karbon tersier, yaitu atom karbon yang mengikat tiga atom karbon
lainnya.
d.
Atom karbon kuartener, yaitu atom karbon yang mengikat empat atom karbon
lainnya
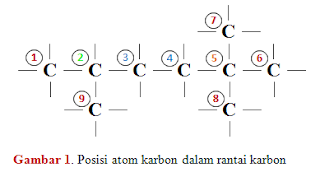
Perhatikan rantai karbon berikut
ini :
Pada gambar di atas atom karbon
yang bernomor 1, 6, 7, 8 dan 9 adalah atom karbon primer, atom karbon yang bernomor 3 dan 4 adalah atom karbon sekunder,
atom karbon yang bernomor 2 adalah atom karbon tersier sedangkan atom karbon yang bernomor 5 adalah atom karbon kuartener.
IDENTIFIKASI SENYAWA KARBON
Untuk mengidentifikasi apakah suatu bahan (zat)
merupakan senyawa karbon atau bukan, dapat dilakukan dengan membakar bahan
(zat) tersebut. Pembakaran tidak sempurna dari senyawa karbon akan menghasilkan
zat sisa berapa arang (jelaga) atau karbon. Sedangkan bila pembakarannya
berlangsung sempurna, akan menghasilkan gas karbon dioksida (CO2).
Keberadaan CO2 dapat diketahui dengan cara
mengalirkannya ke dalam air kapur {larutan Ca(OH)2} atau air barit
{larutan Ba(OH)2. Apabila senyawa yang dibakar merupakan senyawa
karbon (menghasilkan CO2), air kapur atau air barit akan menjadi
keruh.
Reaksi yang terjadi dalam persamaan berikut :
CO2(g)
+ Ca(OH)2 (aq) → CaCO3(s) + H2O(l)
Berdasarkan jenis ikatan antara atom karbon, senyawa
hidrokarbon dapat dibedakan menjadi hidrokarbon jenuh dan tak jenuh.
Seluruh ikatan antar atom karbon pada hidrokarbon jenuh
merupakan ikatan kovalen tunggal. Pada hidrokarbon tak jenuh, terdapat satu
atau lebih ikatan rangkap ataupun ikatan rangkap tiga.
Berdasarkan
bentuk rantai karbon dan jenis ikatannya, senyawa hidrokarbon dikelompokkan
menjadi:
1.
Hidrokarbon alifatik
Hidrokarbon Alifatik
adalah hidrokarbon dengan rantai terbuka dan memiliki ikatan tunggal (jenuh) ataupun ikatan rangkap (tak
jenuh).
Contohnya :
2.
Hidrokarbon alisiklik
Hidrokarbon alisiklik
adalah hidrokarbon dengan rantai tertutup atau melingkar.
Contohnya :
3.
Hidrokarbon aromatik
Hidrokarbon aromatik
adalah hidrokarbon dengan rantai melingkar yang memiliki ikatan konjugasi,
yaitu ikatan tunggal dan ikatan rangkap dua yang berselang-seling.
Contohnya :















Nama :Erlina Ade Liani
BalasHapusKelas :XI MIPA 1
CH₃-CH₂-CH₂-CH₂-CH₂-CH3 ⇒ n-heksana
CH₃-CH-CH₂-CH₂-CH₃ ⇒ 2metil-Pentana
I
CH₃
CH₃-CH₂-CH-CH₂-CH₃ ⇒ 3metil-Pentana
I
CH₃
CH₃-CH-CH-CH₃ ⇒ 2,3 dimetil-butana
I I
CH₃ CH₃
CH₃
I
CH₃-C-CH₂-CH₃ ⇒ 2,2dimetil-Butana
I
CH₃
Komentar ini telah dihapus oleh pengarang.
BalasHapusCH₃-CH₂-CH₂-CH₂-CH₂-CH3 ⇒ n-heksana
BalasHapusCH₃-CH-CH₂-CH₂-CH₃ ⇒ 2metil-Pentana
I
CH₃
CH₃-CH₂-CH-CH₂-CH₃ ⇒ 3metil-Pentana
I
CH₃
CH₃-CH-CH-CH₃ ⇒ 2,3 dimetil-butana
I I
CH₃ CH₃
CH₃
I
CH₃-C-CH₂-CH₃ ⇒ 2,2dimetil-Butana
I
CH₃